
光阴似箭,日月如梭
2023年悄然而至
回首2022
奥泰康深耕业务
与合作伙伴见证成功喜悦
与医疗同仁收获进步果实
让我们跟随时间
回顾2022年共同走过的精彩旅程
1月
January
●神经介入领域新突破
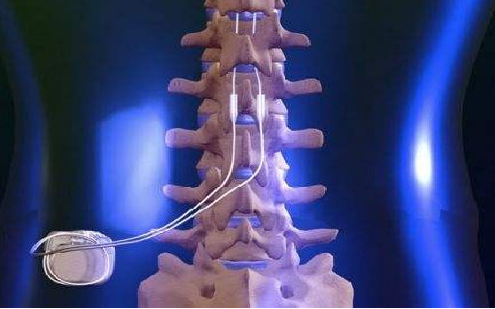
1月,与国内神经调控领域创新型公司合作,开启奥泰康继脑深部电刺激系统(DBS)后的首个用于慢性疼痛的脊髓刺激系统(SCS)临床服务,系神经介入领域的全新突破。
●助力交联透明质酸钠凝胶获证

1月26日,常州百瑞吉生物医药有限公司生产的“交联透明质酸钠凝胶”获国家药监局批准上市,产品用于预防盆腹腔术后粘连,奥泰康助力产品获得市场准入。
2月
February
●9个临床项目会议如期召开

2月,春节后复工投产,临床注册部总计完成9个临床启动会和伦理会,充分保证临床试验项目进度。
3月
March
●反应性闭环神经刺激系统临床植入
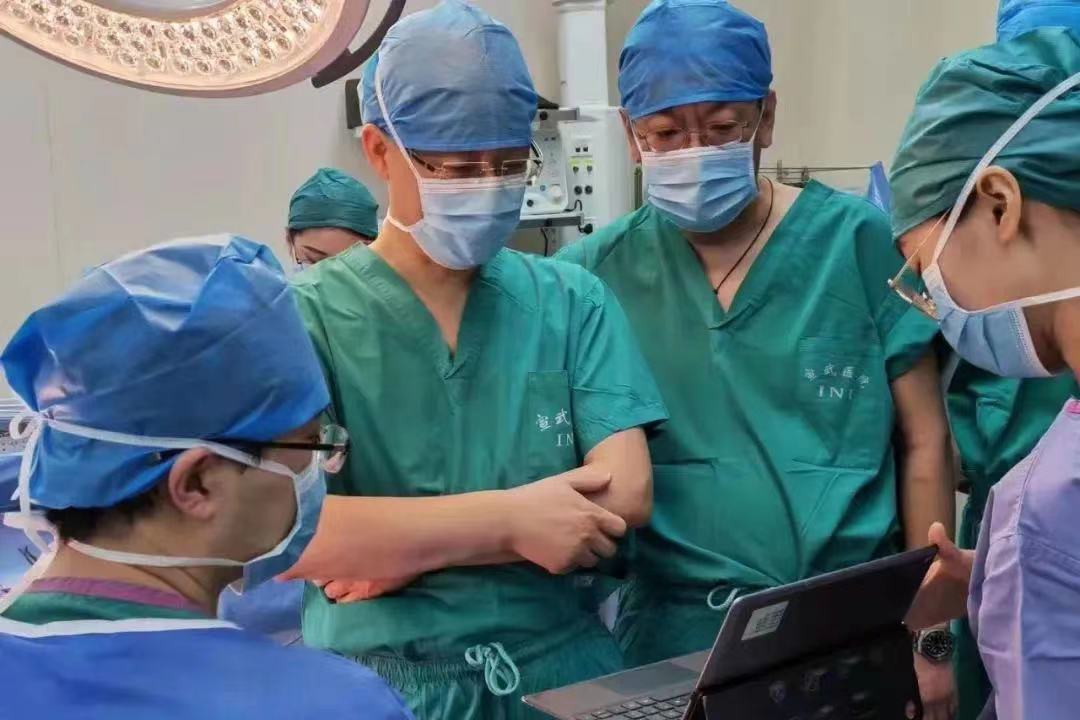
3月9日,首都医科大学宣武医院开展闭环反应性神经刺激系统 Epilcure™注册临床试验植入手术,系国家药监局注册临床试验的首例入组,奥泰康作为CRO服务方,推动具备自主知识产权的“脑机接口”高新技术产品在临床落地。
4月
April
●助力口腔软组织修复膜获证
 4月6日,国家药监局批准博辉瑞进的口腔修复膜上市,产品用于口腔软组织浅层缺损后的覆盖修复,系国内第一张SIS生物材料的口腔软组织修复膜产品,奥泰康负责产品注册申报。
4月6日,国家药监局批准博辉瑞进的口腔修复膜上市,产品用于口腔软组织浅层缺损后的覆盖修复,系国内第一张SIS生物材料的口腔软组织修复膜产品,奥泰康负责产品注册申报。5月
May
●助力两款AI肺结节软件获证

5月6日,奥泰康担任临床试验服务顾问,助力两款CT肺结节辅助诊断软件获国家药监局批准上市。截至目前,奥泰康已深度参与50余个人工智能(AI)临床注册项目,并获得9张三类医疗器械注册证。
●世界首创结构贴合TAVR系统植入
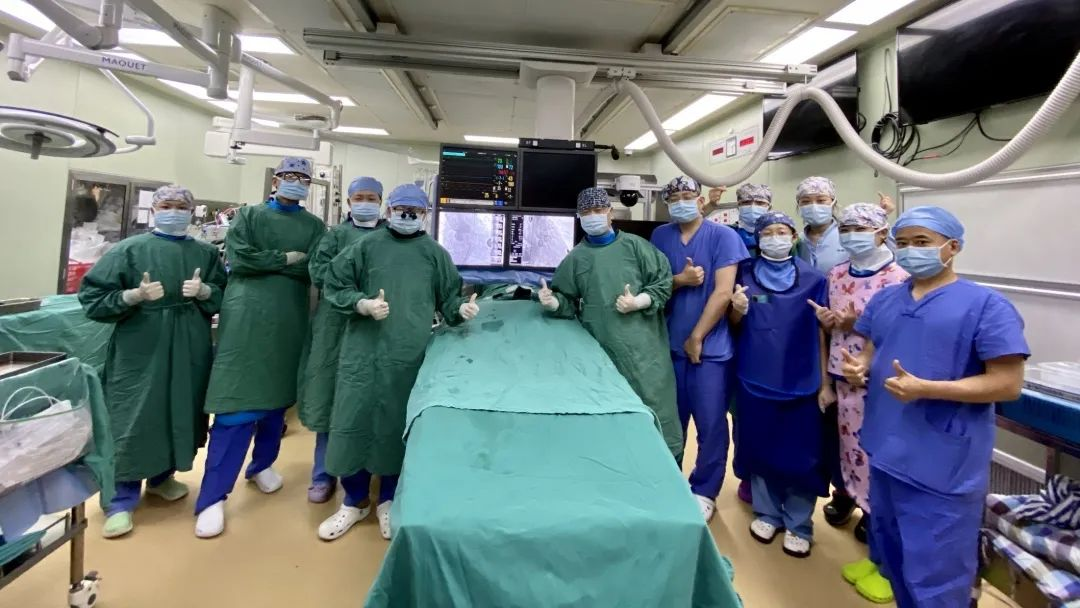
5月20日,四川大学华西医院应用南京圣德研发的带结构贴合锚定及全新释放方式的自膨式TAVR产品Xcor,实施经导管主动脉瓣膜置换手术,系世界首创结构贴合TAVR系统手术在中国的首例植入。
6月
June
●细胞外基质临床试验完成首例入组
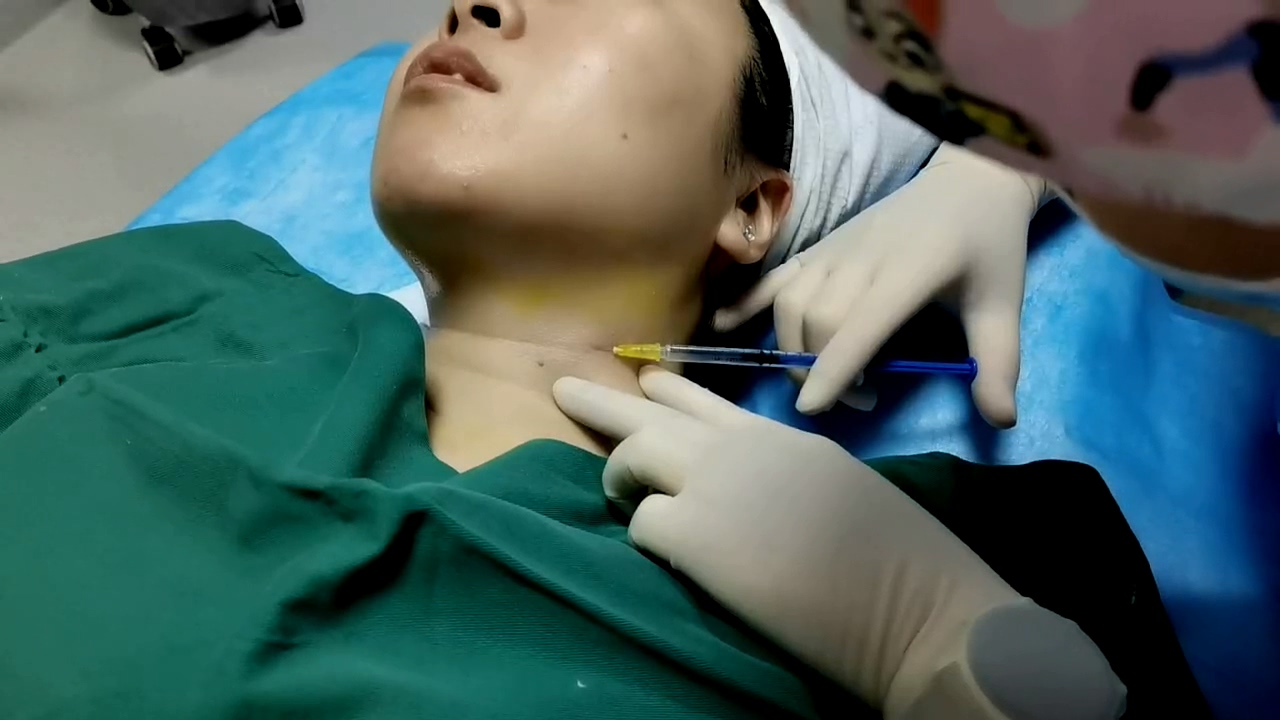 6月,北京CDMO中心细胞外基质临床试验完成首例入组,推动再生医学生物材料新的临床应用,依托细胞外基质技术打造注射填充类医美产品,满足多元化临床需求。
6月,北京CDMO中心细胞外基质临床试验完成首例入组,推动再生医学生物材料新的临床应用,依托细胞外基质技术打造注射填充类医美产品,满足多元化临床需求。7月
July
●经导管三尖瓣产品临床研究启动

7月,厦门大学心血管病医院运用臻亿医疗自主研发的NeoBlazar®经导管三尖瓣夹合器及输送系统实施微创经导管三尖瓣修复术,此次手术系奥泰康作为CRO服务方的NeoBlazar®临床实验全国首例入组。
●CDMO两款产品通过体系核查

7月底,奥泰康CDMO中心两款产品通过北京局组织的质量现场体系核查工作(医用生物凝胶和丝素蛋白贴敷料),标志着CDMO中心已建立健全与所生产医疗器械相适应的质量管理体系并保持其有效运行,产品获得生产许可资质,市场准入迈入关键性进程。
8月
August
●助力吻合口加固修补片获证

8月2日,博辉瑞进研发的创新医疗器械吻合口加固修补片获得药监局批准上市,系全球首款用于管型吻合器的SIS材料吻合口加固修补片,奥泰康负责产品注册申报。
●双波长双通道MRgLITT手术完成
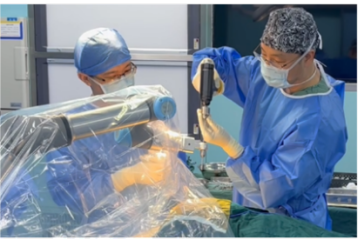
8月6日,奥泰康作为CRO服务方,助力佳量医疗完成我国首例双波长双通道MRgLITT治疗额叶难治性癫痫消融手术,双波长MRgLITT在国内的首次临床应用,标志着国产产品在国际前沿医疗核心技术领域的重大突破。
●CDMO四款产品通过主文档备案
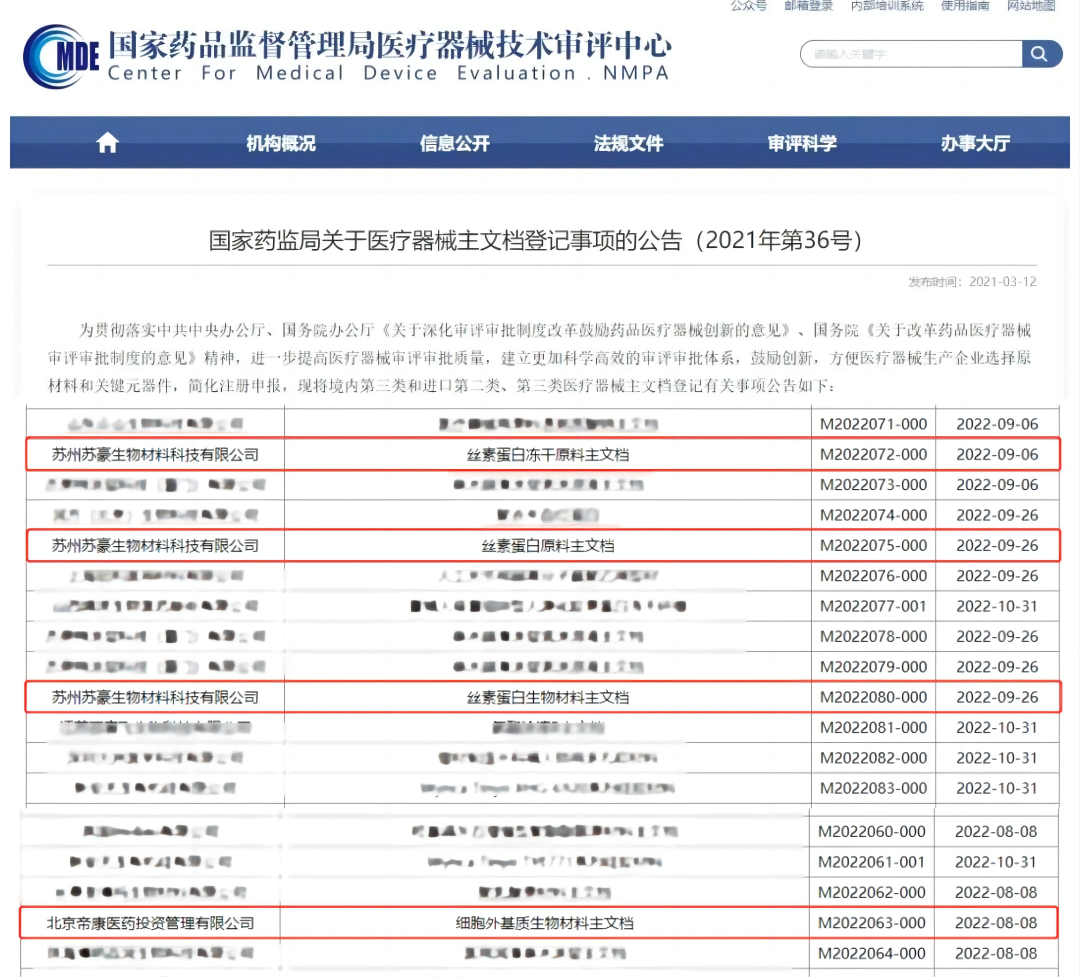
8月,CDMO中心四款医疗器械原材料通过主文档登记备案(丝素蛋白冻干原料、丝素蛋白原料、丝素蛋白生物材料、细胞外基质生物材料),主文档备案的通过为医药行业细胞外基质和丝素蛋白产品研发及生产提供了合法来源的原料,具有里程碑意义。
9月
September
●苏州CDMO申请第14项发明专利

9月15日,苏州CDMO中心申请本年度第14项发明专利,立足丝素蛋白材料,苏州CDMO中心共申请专利近20项,已授权专利9项。
●2022年年会暨颁奖盛典落幕

9月24日,奥泰康【逆势领航,悦见繁华】2022年年会暨颁奖盛典于北京隆重举行,年会回顾了公司过往工作成果,并为优秀获奖员工及管理者颁奖,线上直播平台同步分享盛况。
●植入式眼部肌肉神经刺激器首研会

9月28日,由超目科技发起的多中心临床研究在北京成功召开方案讨论会,奥泰康作为CRO服务方参加会议,方案讨论会的召开标志着产品进入临床试验阶段,产品将为先天性眼球震颤患者带来希望。
10月
October
●助力可吸收丝素修复膜获证

10月13日,湖北赛罗生物材料有限公司自主研发的“可吸收丝素修复膜”获国家药监局批准上市,产品系国内首个获药监局批准上市的、应用于口腔修复的植入类丝素蛋白III类医疗器械产品,奥泰康担任临床注册服务。
●助力第18个创新产品通过创新审查
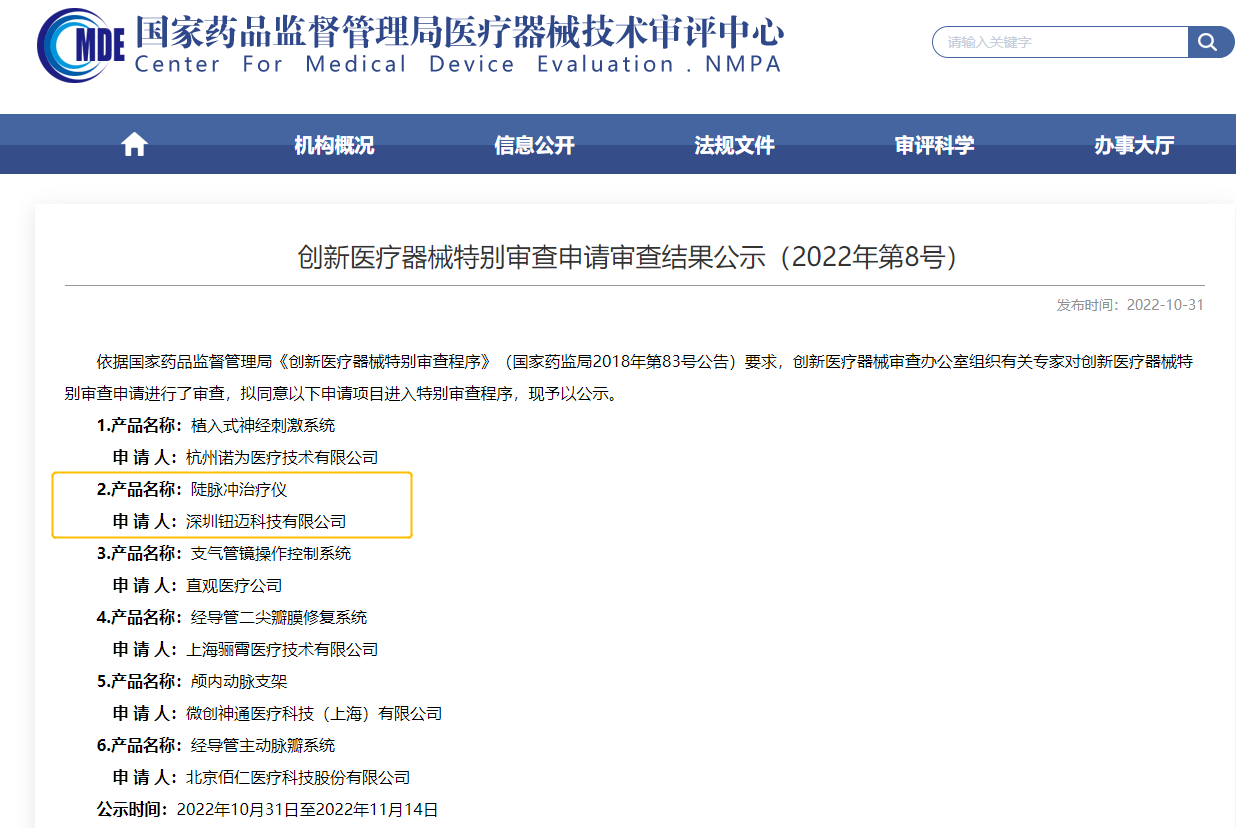
10月31日,深圳钮迈科技研发的创新医疗器械“陡脉冲治疗仪”进入特别审查程序,奥泰康提供创新申报和临床试验服务,系第18项创新产品临床服务。
11月
November
●服务意见征集活动上线

11月24日,感恩节来临之际,奥泰康举办服务意见征集活动,通过线上活动渠道共收集到来自合作伙伴和临床研究者近200份反馈问卷,这些宝贵意见将促使奥泰康不断提高项目质量,优化临床服务。
12月
December
●入围全国工商联医药研发50强

12月8日,全国工商联医药业商会发布2021年度中国医药行业最具影响力榜单,经过专家组成员评选,奥泰康入围2021年度中国医药研发50强榜单。
●公司新版官网即将上线

经过数月筹备与搭建,奥泰康新版官方网站即将上线,届时将以崭新姿态面向医疗同仁,希望医疗各界能够全面了解奥泰康CRO&CDMO一体化服务。
凛冬散尽,星河长明
疫情的阴霾终将逝去
奥泰康依旧不改初心
坚持以优质服务赋能医疗
历尽千帆,不辍前行
新的一年
让我们穿越逆境,抵达繁星!